dipropionato de beclometasona 100 mcg
fumarato de formoterol 6 mcg
Pó para Inalação

Bula Paciente
IDENTIFICAÇÃO DO MEDICAMENTO
FOSTAIR® DPI 100/6
dipropionato de beclometasona 100 mcg
fumarato de formoterol 6 mcg
APRESENTAÇÕES
Pó para inalação.
Embalagem contendo um dispositivo NEXT® DPI, com 120 doses.
Cada dose contém 100 mcg de dipropionato de beclometasona e 6 mcg de fumarato de formoterol.
USO INALATÓRIO POR VIA ORAL
USO ADULTO
Composição:
Cada dose de FOSTAIR® DPI contém:
|
dipropionato de beclometasona............................................................. |
100 mcg |
|
fumarato de formoterol......................................................................... |
6 mcg |
|
Excipiente qsp....................................................................................... |
1 dose |
Excipientes: lactose monoidratada e estearato de magnésio.
INFORMAÇÕES AO PACIENTE
FOSTAIR® DPI, pó para inalação contido em dispositivo NEXT® DPI, é indicado para o tratamento do estreitamento das vias aéreas e da dificuldade de respirar associada às doenças das vias aéreas, como asma e doença pulmonar obstrutiva crônica (DPOC).
Asma:
FOSTAIR® DPI deve ser usado por pessoas:
FOSTAIR® DPI pode ser utilizado como um tratamento de manutenção regular e também em resposta aos sintomas da asma, quando necessário.
FOSTAIR® DPI não é indicado para o tratamento inicial da asma.
DPOC:
FOSTAIR® DPI está indicado no tratamento regular de pacientes com doença pulmonar obstrutiva crônica (DPOC) grave, com sintomas frequentes e história de exacerbações (crises de falta de ar), apesar de tratamento com broncodilatadores (medicação de alívio da falta de ar).
FOSTAIR® DPI é um medicamento em pó para a inalação oral (pela boca) que contém duas substâncias ativas: o dipropionato de beclometasona e o fumarato de formoterol.
O dipropionato de beclometasona pertence a um grupo de medicamentos chamado corticosteroides e age diminuindo a inflamação, inchaço e irritação das vias aéreas inferiores.
O fumarato de formoterol pertencente ao grupo de medicamentos chamado broncodilatadores de ação prolongada, que ajuda a aumentar o calibre das vias aéreas.
A ação do fumarato de formoterol (broncodilatação) ocorre rapidamente, de 1 a 3 minutos após a inalação. Porém, o efeito sinérgico dos dois princípios ativos só será percebido após alguns dias de tratamento.
Os dois princípios ativos facilitam a respiração ao aliviar os sintomas de falta de ar, chiado no peito e tosse em pacientes com asma e DPOC e também ajudam a prevenir os sintomas da asma.
Você não deve utilizar o medicamento se for alérgico aos princípios ativos ou quaisquer componentes da formulação ou se você for alérgico a outros medicamentos usados para tratamento da asma.
Você não deve utilizar o medicamento se estiver apresentando sintomas agudos da asma como falta de ar, chiado e tosse, se sua asma estiver piorando ou se você estiver apresentando crise aguda de asma. Nesse caso, você deve usar o medicamento de resgate de ação rápida, o qual deve ser carregado por você a todo o momento.
Este medicamento é contraindicado para menores de 18 anos.
Com o propósito de se obter um efeito terapêutico total e eficaz do tratamento, torna-se indispensável que você siga rigorosamente as instruções relativas à forma de inalação de FOSTAIR® DPI.
Sempre utilize FOSTAIR® DPI exatamente como indicado pelo seu médico. Procure seu médico ou o farmacêutico caso você tenha dúvidas.
É importante você consultar seu médico regularmente. Ele fará exames para garantir que você está utilizando a dose ideal de FOSTAIR® DPI e ajustará seu tratamento à dose mais baixa que melhor controle seus sintomas.
Sob nenhuma circunstância você deve mudar a dose sem primeiro conversar com seu médico.
Se achar que o medicamento não está sendo eficaz, sempre converse com seu médico antes de aumentar a dose.
Não reduza a dose ou suspenda a medicação sem orientação do seu médico. Mesmo ao se sentir melhor, não pare de utilizar FOSTAIR® DPI nem reduza a dose. Se quiser fazê-lo, converse com seu médico. É muito importante que você use FOSTAIR® DPI regularmente mesmo se não apresentar mais sintomas.
Se achar mais difícil respirar após usar o dispositivo, pare de usá-lo imediatamente e procure assistência médica.
Se seus sintomas piorarem ou se tornarem mais difíceis de controlar (p.ex. caso você use seu dispositivo de "resgate" com mais frequência), você deve ser examinado por seu médico. Se seu dispositivo de "resgate" não melhorar seus sintomas, procure seu médico imediatamente. Sua doença pode ter piorado e seu médico pode precisar alterar sua dose ou prescrever outro medicamento.
Precauções:
Sempre informar o médico, nos casos de:
Como os corticosteroides podem apresentar propriedades imunossupressoras, caso você tenha recebido vacina recentemente, informe o seu médico.
O tratamento com beta2-agonista, como formoterol contido no FOSTAIR® DPI, pode causar uma queda acentuada no nível de potássio sérico (hipocalemia), cujos sintomas são: tonturas, fadiga, paralisias, falta de ar, dor muscular, obstipação intestinal e cãibras.
Se você tem asma severa, deve ter atenção redobrada. Isso se deve ao fato de que a falta de oxigênio no sangue e outros tratamentos os quais o paciente pode estar utilizando tornam esse efeito mais forte (vide "interações medicamentosas").
Caso você esteja utilizando altas doses de corticosteroides inalados por períodos longos, pode ser necessário o aumento de dose de corticosteroides habitualmente utilizados em situações de emergência (hospitalização após um acidente, ferimento grave ou antes de uma operação, por exemplo). Nesse caso, seu médico deve ser informado para decidir a necessidade de aumentar sua dose e pode prescrever esteroide em comprimidos ou injetável.
Alguns estudos científicos têm indicado que o formoterol, um dos componentes presentes no FOSTAIR® DPI, pode aumentar o risco de morte relacionado à asma. Em caso de dúvida, procure seu médico.
Caso você precise ir ao hospital, lembre-se de levar todos os seus medicamentos e dispositivos com você, incluindo FOSTAIR® DPI e qualquer outro medicamento comprado sem prescrição, em sua embalagem original, se possível.
Antes de iniciar outro tratamento, converse com o seu médico ou farmacêutico se você estiver usando ou se usou recentemente outros medicamentos, incluindo qualquer outro dispositivo e medicamentos obtidos sem prescrição médica. Isto porque FOSTAIR® DPI pode interferir no modo de ação de alguns outros medicamentos e, além disso, alguns medicamentos podem interferir no modo de ação do FOSTAIR® DPI.
Não utilizar betabloqueadores, usados para tratar diversos problemas no coração, hipertensão e glaucoma (pressão aumentada nos olhos), com este medicamento. Se você precisar usar betabloqueadores (inclusive colírio), o efeito do formoterol pode se tornar reduzido ou o formoterol pode, inclusive, não fazer nenhum efeito.
Distúrbio visual: se você apresentar alterações na visão ou sintomas como visão turva, informe seu médico para avaliação de possíveis causas que podem incluir catarata, glaucoma ou doenças raras que têm sido notificadas após o uso de corticosteroides sistêmicos e tópicos.
Gravidez e lactação:
Não há dados clínicos sobre mulheres usando o FOSTAIR® DPI durante a gravidez.
Se estiver grávida, converse com seu médico antes de usar este medicamento. Você deve usar FOSTAIR® DPI somente se seu médico achar que os benefícios do medicamento para você são superiores a qualquer risco potencial à sua criança. Isso se aplica especialmente aos primeiros três meses de gravidez. Não se deve utilizar este medicamento enquanto estiver em período de amamentação, salvo se seu médico achar que os benefícios são superiores a qualquer risco potencial à sua criança.
Converse com seu médico ou farmacêutico antes de utilizar/usar qualquer medicamento.
Uso em idosos:
Não é necessário ajuste de dose para pacientes idosos.
Uso em crianças:
Não está indicado para uso em crianças.
Uso em pacientes com insuficiência hepática e renal:
Não há dados disponíveis sobre o uso de FOSTAIR® DPI em pacientes com comprometimento hepático ou renal.
Efeitos sobre a capacidade de conduzir e utilizar máquinas:
É improvável que FOSTAIR® DPI cause qualquer efeito sobre a capacidade de dirigir e operar máquinas. Porém, se você apresentar eventos adversos como tontura e tremor, sua capacidade em conduzir ou operar máquinas pode ficar prejudicada.
Informações importantes sobre outros componentes de FOSTAIR® DPI
FOSTAIR® DPI para inalação contém lactose (um tipo de açúcar). Se você apresenta intolerância a certos tipos de açúcar, entre em contato com seu médico antes de usar este medicamento.
Interações medicamentosas:
Antes de iniciar o tratamento, avise seu médico ou farmacêutico caso esteja tomando ou tenha tomado qualquer outro medicamento, incluindo medicamentos obtidos sem prescrição do seu médico.
O medicamento FOSTAIR® DPI possui interação medicamentosa com os betabloqueadores (medicamentos usados para tratar várias doenças, incluindo problemas cardíacos, pressão alta e glaucoma, que é o aumento da pressão nos olhos). Se você precisar utilizar betabloqueadores (incluindo colírios), o efeito do formoterol pode ficar menor ou ele pode perder a eficácia. Por outro lado, o uso de outros medicamentos beta-adrenérgicos (que também são usados na asma) pode potencializar os efeitos do formoterol.
A utilização concomitante de FOSTAIR® DPI com os medicamentos abaixo pode causar:
Você deve evitar ingerir bebidas alcoólicas a menos que tenha falado com seu médico primeiro, pois o álcool pode reduzir a tolerância do seu coração ao formoterol.
Alguns medicamentos podem aumentar os efeitos de FOSTAIR® e o seu médico pode querer monitorá-lo cuidadosamente se você estiver utilizando estes medicamentos (incluindo alguns medicamentos para o HIV: ritonavir, cobicistate).
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Uso criterioso no aleitamento ou na doação de leite humano. O uso deste medicamento no período da lactação depende da avaliação e acompanhamento do seu médico ou cirurgião-dentista.
Esse medicamento pode causar resultado positivo em testes antidopagem em atletas. Consulte a Lista Proibida vigente, Código Mundial Antidopagem disponível no endereço eletrônico da Autoridade Brasileira de Controle de Dopagem para mais informações.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Este medicamento pode aumentar o risco de alteração grave nos batimentos cardíacos, que pode ser potencialmente fatal (morte súbita).
Não tome este medicamento se você tiver uma alteração no coração chamada síndrome congênita de prolongamento do intervalo QT (ou síndrome do QT longo), ou se você já teve algum episódio de ritmo cardíaco anormal, porque pode ser perigoso e provocar alterações do ritmo do coração, inclusive com risco de morte.
Avise seu médico se você tiver bradicardia (diminuição da frequência cardíaca), insuficiência cardíaca ou outras doenças do coração, ou se você souber que tem baixo nível de potássio ou de magnésio no sangue. Avise seu médico se você estiver utilizando outros medicamentos, especialmente medicamentos que causam prolongamento do intervalo QT (alteração do ritmo do coração no eletrocardiograma), medicamentos para arritmia (para corrigir o ritmo do coração) ou medicamentos diuréticos (remédios para eliminar água do corpo).
Não remova o dispositivo do cartucho e do envelope de alumínio até o momento do uso.
Mantenha a tampa do dispositivo inalatório fechada nos intervalos entre as doses. Quando não estiver usando seu dispositivo, mantenha-o limpo e em local seco.
Conservar o medicamento FOSTAIR® DPI em temperatura ambiente (15 ºC a 30ºC) e proteger da umidade.
FOSTAIR® DPI é um dispositivo multidose de plástico (dispositivo NEXT® DPI) com pó branco e inodoro (sem cheiro).
Depois de aberto, este medicamento deve ser utilizado em 2 meses.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido.
Para a sua segurança, mantenha o medicamento na embalagem original.
Antes de usar, observe o aspecto do medicamento.
Caso você observe alguma mudança no aspecto do medicamento que ainda esteja no prazo de validade, consulte o médico ou o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
LEIA ATENTAMENTE AS INSTRUÇÕES PARA O USO CORRETO. SE NECESSÁRIO, CONSULTE O SEU MÉDICO PARA OBTER EXPLICAÇÕES MAIS DETALHADAS.
Instruções de Uso do Dispositivo NEXT® DPI:
Não remova o dispositivo do cartucho e do envelope de alumínio se você não pretende usá-lo imediatamente.
Use o medicamento conforme indicado.
Se você não tiver certeza se sua dose está correta, entre em contato com seu médico ou farmacêutico.
Mantenha a tampa do dispositivo inalatório fechada nos intervalos entre as doses.
Quando não estiver usando seu dispositivo, mantenha-o limpo e em local seco.
Não tente abrir ou desmontar seu dispositivo em hipótese alguma, pois isso irá danificar o dispositivo e o medicamento ficará inadequado ao uso.
Não use seu dispositivo (NEXT® DPI): após a data de validade, se estiver aberto por mais de 2 meses, se estiver quebrado, se o contador de doses mostrar “0”, se você não conseguir ler o contador de doses.
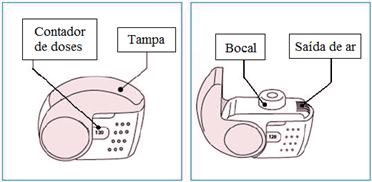
Para administrar uma dose do seu dispositivo NEXT® DPI são necessários apenas três simples passos: abrir, inalar e fechar.
Antes de usar seu dispositivo pela primeira vez:
Como usar seu dispositivo
Inspeção visual
Abrir
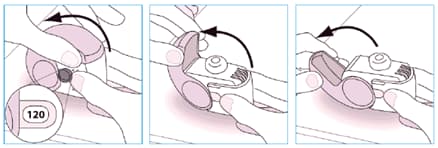
Inalar
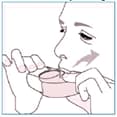
Sempre que possível, ficar de pé ou sentar-se em posição vertical quando for utilizar o medicamento.
Fechar

Caso necessite de outra dose, manter o dispositivo na posição vertical e repetir as etapas 1 a 12.
ATENÇÃO: Com NEXT® DPI o medicamento apenas se torna disponível para inalação quando a tampa estiver completamente aberta. Abrir a tampa, inalar e fechar a tampa fazem parte do mecanismo de liberação e contagem dos acionamentos (doses). Por isso, você deve fechar a tampa do dispositivo completamente todas as vezes que fizer uso do medicamento. Se você não tiver inalado o medicamento através do dispositivo, o número de acionamentos (doses) mostrados no dispositivo não diminui ao fechar a tampa.
Para diminuir o risco de uma infecção fúngica na boca e garganta e alteração da voz, enxágue sua boca com água após cada inalação.
Se achar que o efeito de FOSTAIR® DPI é muito forte ou muito fraco, diga isso ao seu médico ou farmacêutico.
Se você tem dificuldade de respirar e ela piorou ou o tornou ofegante (você respira com um som de assobio), logo após a inalação, pare o tratamento imediatamente e procure seu médico.
Isso é causado pelo estreitamento das vias aéreas (broncoespasmo) em seus pulmões e pode ocorrer ao usar um dispositivo.
Limpeza:
Normalmente, não é necessário limpar seu dispositivo. Porém, sempre que necessário, por exemplo, você verificou presença de saliva no dispositivo após a inalação, você pode limpar seu dispositivo após o uso com um pano seco. Não use água ou outros líquidos para limpar o dispositivo. Mantenha-o seco.
Posologia:
FOSTAIR® DPI deve somente ser utilizado por via inalatória (oral).
Em relação à duração do tratamento, seguir as orientações do seu médico.
As doses serão ajustadas pelo médico em cada caso.
FOSTAIR® DPI libera uma formulação extrafina que resulta em uma maior quantidade do medicamento nos pulmões, quando comparado com formulações não extrafinas. Portanto, se você fazia uso de outra medicação contendo dipropionato de beclometasona, em formulação não extrafina, e agora irá fazer uso de FOSTAIR® DPI, seu médico poderá prescrever uma dose menor de dipropionato de beclometasona, se comparado ao medicamento anteriormente utilizado. Entretanto, se você fazia uso da formulação em aerossol (FOSTAIR® aerossol) e agora irá fazer uso de FOSTAIR® DPI não é necessário ajuste de dose. Você deve utilizar o medicamento de acordo com a orientação do seu médico.
Seu médico lhe fará regularmente um check-up a fim de certificar-se de que você esteja usando a dose correta. Uma vez que sua asma esteja bem controlada, seu médico pode considerar apropriado reduzir a dose de FOSTAIR® DPI. Você não deve, sob nenhuma circunstância, alterar sua dose sem antes falar com seu médico.
Doses Recomendadas:
Uso adulto
Asma:
Fostair® DPI pode ser prescrito pelo seu médico para duas diferentes formas de uso:
A - Terapia de Manutenção:
Utilize Fostair® DPI todos os dias para tratar sua asma, em conjunto com um medicamento de alívio rápido isolado (tratamento de resgate) para tratar a piora repentina dos sintomas da asma, como falta de ar, chiado e tosse.
Recomenda-se utilizar de 1 ou 2 inalações, a cada 12 horas (duas vezes ao dia).
A dose máxima diária é de 4 inalações.
Não aumente a dose.
Se você sentir que este medicamento não é eficaz, sempre converse com seu médico antes de aumentar a dose.
Lembre-se de sempre andar com o seu medicamento de resgate para tratar os sintomas de piora da asma ou uma crise súbita de asma.
B - Terapia de Manutenção e Alívio:
Utilize Fostair® DPI todos os dias para tratar sua asma e também utilize Fostair® DPI para tratar a piora repentina dos sintomas da asma, como falta de ar, chiado e tosse.
Recomenda-se utilizar 1 inalação, a cada 12 horas (duas vezes ao dia), sendo essa a terapia de manutenção, ou seja, você deve usar o medicamento dessa maneira todos os dias, mesmo que você não apresente sintomas de asma.
Você também deve utilizar Fostair® DPI para tratar a piora repentina dos sintomas da asma. Se você apresentar sintomas da asma, utilize 1 inalação adicional e aguarde alguns minutos. Caso você não se sinta melhor, utilize mais 1 inalação.
Não utilize mais de 6 inalações para alívio dos sintomas ao dia, pois a dose máxima do medicamento para tratamento de manutenção e alívio é de 8 inalações por dia.
Caso você sinta que precisa de mais inalações ao dia para controlar seus sintomas da asma, entre em contato com seu médico para obter sua recomendação. Ele pode alterar seus tratamentos.
DPOC:
Recomenda-se utilizar 2 inalações, a cada 12 horas (duas vezes ao dia).
A dose máxima diária é de 4 inalações.
Pacientes sob riscos:
Pessoas idosas não precisam de ajuste de dose.
FOSTAIR® DPI não é recomendado para uso em crianças.
Mesmo que esteja se sentindo melhor, não interrompa o tratamento com FOSTAIR® DPI ou diminua a dose. Caso queira fazer isso, converse com seu médico antes. É muito importante para você usar FOSTAIR® DPI todos os dias como prescrito pelo seu médico, mesmo que você não apresente mais sintomas.
Se os seus sintomas não melhorarem após o uso de FOSTAIR® DPI, você pode estar usando-o incorretamente. Portanto, verifique as instruções de uso corretamente ou entre em contato com seu médico para ele lhe ensinar como usar o dispositivo outra vez.
Se os seus sintomas piorarem ou estiverem difíceis de controlar (por exemplo, se estiver usando sua medicação de resgate com mais frequência) ou se sua medicação de resgate não estiver melhorando seus sintomas, você deve continuar usando FOSTAIR® DPI, mas deve procurar seu médico o quanto antes. Seu médico pode precisar mudar sua dose de FOSTAIR® DPI ou prescrever medicamentos adicionais.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
Informe ao seu médico ou cirurgião-dentista o aparecimento de sintomas novos, agravação de sintomas atuais ou retorno de sintomas antigos.
O uso inadequado do medicamento pode mascarar ou agravar sintomas.
Consulte um médico regularmente. Ele avaliará corretamente a evolução do tratamento. Siga corretamente suas orientações.
Se esquecer de usar FOSTAIR® DPI utilize o medicamento logo que lembrar. Se for quase hora da dose seguinte, não utilize a dose faltante, apenas utilize a próxima dose no próximo horário. Não dobre a dose.
Em caso de dúvidas, procure a orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Uma vez que FOSTAIR® DPI contém dipropionato de beclometasona e fumarato de formoterol, o tipo e severidade das reações adversas associadas a cada composto podem ser previstos. Não há incidência de eventos adversos adicionais após a administração concomitante dos dois compostos.
Reações adversas reportadas durante os estudos clínicos e experiência clínica com FOSTAIR® DPI:
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): Não foram relatadas reações muito comuns até o momento.
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): pneumonia (em pacientes com DPOC), tremores.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento): nasofaringite (inflamação da mucosa nasal), candidíase na boca, hipertrigliceridemia (aumento de triglicérides no sangue), dor de cabeça, aumento ou diminuição dos batimentos do coração, angina pectoris (dor no coração), isquemia do miocárdio (falta de oxigênio no coração), irritação na garganta, crise asmática, dispneia (falta de ar), dor orofaríngea, disfonia (alteração da voz), tosse, náusea, fadiga, irritabilidade, alterações em eletrocardiograma (prolongamento do intervalo QT e/ou progressão lenta da onda R), diminuição de cortisol livre na urina, diminuição da concentração de cortisol no sangue, aumento do potássio no sangue, aumento da glicose sanguínea.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento): Não foram relatadas reações raras até o momento.
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento): Não foram relatadas reações muito raras até o momento.
Reação cuja frequência é desconhecida: hiperatividade psicomotora, distúrbios do sono, ansiedade, depressão, agressividade, mudanças comportamentais (predominantemente em crianças), visão turva.
Reações adversas típicas associadas ao uso de formoterol:
Dentre as reações adversas observadas, aquelas tipicamente associadas ao formoterol são: tremores, dores de cabeça, aumento ou diminuição dos batimentos do coração, dor no coração (angina pectoris), falta de oxigênio no coração (isquemia do miocárdio), prolongamento do intervalo QT. Reações adversas não observadas na experiência clínica com doses terapêuticas de FOSTAIR® DPI, mas tipicamente associadas com a administração de medicamentos da mesma classe do formoterol são: palpitações, alterações no batimento do coração (fibrilação atrial, extrassístole ventricular, taquiarritmia), níveis baixos de potássio e aumento ou diminuição da pressão sanguínea. Insônia, tontura, inquietação e ansiedade têm sido ocasionalmente reportadas durante terapia inalatória com formoterol. Formoterol pode também induzir cãibras e dores musculares.
Reações adversas típicas associadas ao uso de beclometasona:
As reações adversas tipicamente associadas à administração de dipropionato de beclometasona são: nasofaringite, candidíase oral, disfonia, irritação da garganta, irritabilidade, diminuição de cortisol livre na urina, diminuição da concentração sanguínea de cortisol, aumento da glicemia. Reações adversas não observadas na experiência clínica com doses terapêuticas de FOSTAIR® DPI, mas tipicamente associadas com a administração de dipropionato de beclometasona são: infecção fúngica oral e pneumonia. Distúrbio de paladar tem sido ocasionalmente reportado durante a terapia com corticoide inalatório.
Pneumonia: informe seu médico se você notar os seguintes sintomas: aumento na produção de expectoração, aumento na coloração da expectoração, febre, aumento da tosse, aumento dos problemas respiratórios.
Usar altas doses de corticosteroides inalatórios por um longo período pode ocasionar:
Assim como ocorre com outras terapêuticas inalatórias, podem surgir espasmos da musculatura bronquial (broncoespasmos paradoxais). Eles são caracterizados pela presença de sons em sibilos (chiados no peito), que aparecem quando você respira imediatamente após o processo da inalação da medicação, e por piora da tosse. Caso isso ocorra, interrompa o tratamento e procure imediatamente seu médico.
Informe seu médico imediatamente se você apresentar reações alérgicas, que incluem: alergias na pele, coceira, erupções na pele, vermelhidão ou inchaço da pele e de mucosas, especialmente dos olhos, da face, lábios e garganta.
Reações adversas reportadas para medicamento semelhante contendo a associação de dipropionato de beclometasona e formoterol:
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): não foram relatadas reações muito comuns até o momento.
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): faringite, candidíase oral, pneumonia (em pacientes com DPOC), cefaleia, rouquidão.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento): gripe, infecção fúngica oral, candidíase orofaríngea, esofágica e vulvovaginal, gastroenterite, sinusite, rinite, granulocitopenia, dermatite alérgica, hipocalemia, hiperglicemia, inquietação, tontura, tremor, otite (infecção no ouvido), palpitações, eletrocardiograma com prolongamento do intervalo QT corrigido, alteração em eletrocardiograma, taquicardia, taquiarritmia, fibrilação atrial (um tipo de arritmia do coração), hiperemia, rubor, tosse, tosse produtiva, irritação na garganta, crise asmática, diarreia, boca seca, dispepsia, disfagia, sensação de queimação nos lábios, náusea, disgeusia (alteração no paladar), prurido, erupção cutânea, hiperidrose (sudorese excessiva), urticária, câimbra muscular, mialgia (dores musculares), proteína C-reativa elevada, contagem de plaquetas elevada, aumento nos ácidos graxos livres, aumento na insulina sanguínea, aumento de corpos cetônicos sanguíneos, diminuição do cortisol sanguíneo.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento): extrassístole ventricular (contração prematura do ventrículo do coração), angina pectoris (dor no coração), broncoespasmo paradoxal, angioedema, nefrite (inflamação nos rins), aumento na pressão sanguínea, diminuição da pressão sanguínea.
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento): trombocitopenia, reações de hipersensibilidade, incluindo eritema, edema nos lábios, face, olhos e faringe, supressão adrenal, catarata, glaucoma, dispneia (falta de ar), exacerbação da asma, retardo no crescimento em crianças e adolescentes, edema periférico, diminuição da densidade óssea.
Reação cuja frequência é desconhecida: hiperatividade psicomotora, distúrbios do sono, ansiedade, depressão, agressividade, mudanças comportamentais (predominantemente em crianças), visão turva.
Todas as reações adversas descritas acima podem ocorrer durante o uso de FOSTAIR® DPI. Caso você apresente algumas destas reações ou apresente qualquer outra reação não descrita, informe seu médico, cirurgião-dentista ou farmacêutico.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento.
Informe a empresa sobre o aparecimento de reações indesejáveis e problemas com este medicamento, entrando em contato através do serviço de atendimento ao consumidor (SAC).
Se você usar uma quantidade maior do que deveria de FOSTAIR® DPI entre em contato com seu médico ou vá a um hospital mais próximo para receber instruções. Leve seu medicamento com você. Reações adversas podem ocorrer. Informe seu médico caso sinta qualquer sintoma não usual. Seu médico pode querer alguns exames ou decidir as melhores medidas a serem adotadas.
Se você utilizar mais formoterol do que deveria pode ter os seguintes efeitos: sensação de enjoo, aceleração dos batimentos do coração, palpitações, distúrbios do ritmo cardíaco, certas alterações no eletrocardiograma, cefaleia, tremor, sensação de sono, baixos níveis de potássio no sangue, altos níveis de glicose no sangue. Já o uso excessivo de dipropionato de beclometasona pode resultar em uma diminuição temporária do funcionamento de suas glândulas adrenais. Não é necessária ação emergencial uma vez que a função adrenal se recupera em poucos dias.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações sobre como proceder.
DIZERES LEGAIS:
Registro nº 1.0058.0114
Registrado e Importado por:
Chiesi Farmacêutica Ltda.
Rua Dr. Giacomo Chiesi nº 151 - Estrada dos Romeiros km 39,2
Santana de Parnaíba - S.P.
CNPJ n° 61.363.032/0001-46 - ® Marca Registrada
SAC (Serviço de Atendimento ao Consumidor): 0800 1104525
www.chiesi.com.br
Produzido por: Chiesi Farmaceutici S.p.A – Parma – Itália ou Chiesi SAS - La Chaussée Saint Victor - França
Embalado (embalagem secundária) por: Chiesi Farmaceutici S.p.A - Parma – Itália, ou Chiesi SAS - La Chaussée Saint Victor - França ou Chiesi Farmacêutica Ltda. - Santana de Parnaíba - S.P.
Venda sob prescrição
Esta bula foi aprovada pela Anvisa em 06/01/2025
FOSTAIR_DPI_100580114_VP08